Essai Clinique
Les antibiotiques ont été utilisés avec une efficacité relativement bonne comme traitement prophylactique dans la cirrhose décompensée. Cependant, ces stratégies non sélectives entraînent une résistance accrue des bactéries aux antibiotiques les plus couramment utilisés. La rifaximine (RFX), un antibiotique présentant une faible absorption intestinale, semble être une bonne alternative dans de nombreuses maladies gastro-intestinales. Cependant, des études évaluant l’effet de la rifaximine sur l’évolution de la maladie hépatique ont donné des résultats contradictoires, montrant des effets préventifs majeurs chez certains patients, mais aucun effet mesurable chez d’autres patients. Nous planifions donc un essai clinique combinant la rifaximine et l’albumine afin de clarifier l’effet de cet antibiotique chez les patients cirrhotiques.
L’albumine (ALB) est maintenant reconnue comme une protéine extrêmement importante dans les maladies du foie, tant sur le plan diagnostic que thérapeutique. La mesure des concentrations sériques d’albumine contribue en effet à préciser le diagnostic du stade de la maladie hépatique, puisque certains patients atteints de cirrhose décompensée peuvent perdre plus de 2 g d’albumine sérique circulante par jour dans leur intestin, très probablement à cause de fuites dues à une perméabilité accrue de l’intestin. L’albumine est également utilisée comme agent thérapeutique standard pour traiter la cirrhose décompensée. Par exemple, le traitement à l’albumine est recommandé dans des situations cliniques spécifiques, telles que le “syndrome hépatorénal”, la “péritonite d’origine bactérienne” et la “ponction d’ascite de grands volumes” (retrait de plusieurs litres d’ascite).
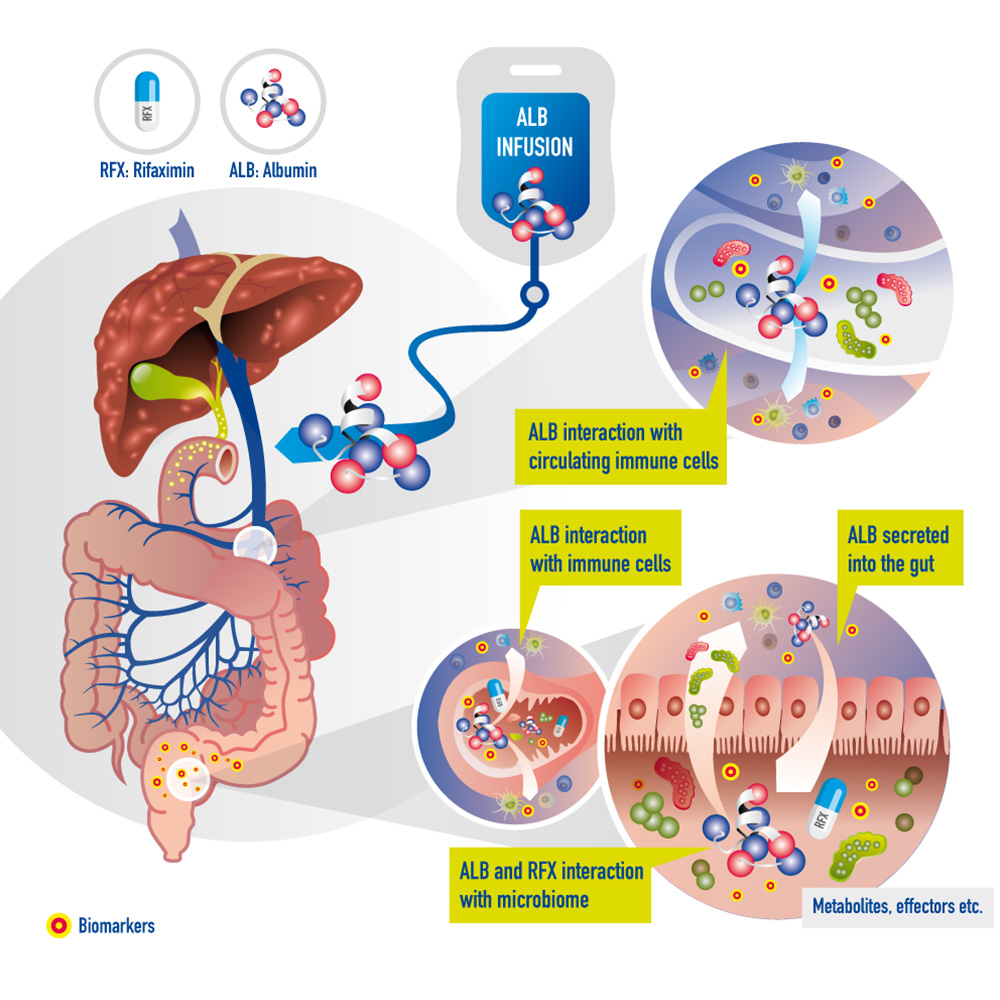
Interaction de la rifaximine et de l'albumine humaine avec le microbiome d’un patient cirrhotique. La rifaximine est administrée par voie orale, tandis que l'albumine humaine est perfusée, mais elle est également excrétée dans la lumière intestinale. Les biomarqueurs issus des analyses du microbiome pourraient refléter précocement la réponse à ces traitements.
Le rôle immunomodulateur de l’albumine n’a été découvert que récemment, dans une étude mettant en évidence un mécanisme par lequel l’albumine pourrait améliorer l’immunité dans la cirrhose du foie (publication originale). Jusqu’à présent, les tentatives de stratification des patients en utilisant l’albumine ont échoué, et de nouveaux outils pour prédire la réponse thérapeutique à l’albumine humaine sont nécessaires de toute urgence. De plus, l’albumine et d’autres molécules qui s’infiltrent dans la lumière intestinale peuvent influencer et être métabolisées par le microbiome intestinal. Une fuite d’albumine dans la lumière intestinale peut altérer le microbiome du patient, avec des répercussions potentielles sur sa physiologie. D’autre part, les métabolites de l’albumine peuvent être absorbés et affecter le patient, en altérant potentiellement son microbiome intestinal et modifiant ainsi ses équilibres biochimiques au niveau systémique (voir illustration ci-dessous).
MICROB-PREDICT analysera non seulement les marqueurs de la réponse des patients au traitement à l’albumine, mais permettra également d’obtenir des résultats significatifs et uniques en utilisant des études précliniques in vitro et in vivo pour comprendre l’interaction de l’albumine avec le microbiote. Enfin, MICROB-PREDICT validera une signature de biomarqueurs, qui permettra de prédire la réponse à l’albumine humaine, dans le cadre d’un essai clinique randomisé (ALB-TRIAL) visant à fournir des conseils sur l’utilisation de l’albumine chez les patients atteints de cirrhose décompensée dans une approche médicale personnalisée.